El gold standard para establecer el control metabólico ha sido clásicamente la hemoglobina glicosilada (A1c), valor promedio de los niveles de glucemia del paciente en los últimos tres meses. Sin embargo este método presenta varias limitaciones necesarias de identificar. Por un lado, la falta de estandarización de la técnica y su baja confiabilidad ante condiciones como anemia, poliglobulia, insuficiencia renal e insuficiencia hepática, entre otras.1,2
Adicionalmente, la A1c no permite identificar las excursiones o variaciones intradía ni interdía de la glucemia, eventos agudos como hipoglucemia o hiperglucemia postprandial, la cual se ha vinculado tanto a repercusiones micro como macrovasculares. 3
Otro método habitual para el control de la glucemia es el automonitoreo glucémico (AMG), que mediante digito punción permite la determinación de la glucosa capilar. Sin embargo, esta determinación es unitemporal, y por tanto la información ofrecida depende del número de controles realizados por el paciente. En los estudios clínicos controlados en los que se utilizó AMG, la reducción de la A1c y de la variabilidad de la glucosa se observó en pacientes que realizaban más de cinco controles por día, condición no habitual en la mayoría de los pacientes.4,5
El ingreso de la tecnología aplicada a la diabetes, en estudios clínicos y posteriormente en la práctica clínica habitual, ha revolucionado la toma de decisiones en pacientes con diabetes.
Una de las tecnologías en diabetes es el CGM, por su siglas en inglés Continuous Glucose Monitoring o Monitoreo Continuo de Glucosa.
Hace tan solo 20 años el uso de CGM se limitaba a la investigación clínica. Recientemente se integró a la práctica clínica habitual, con un uso exponencial de esta tecnología. De acuerdo a datos de publicación recientes, aproximadamente el 30% de los pacientes con DM1 utilizaron CGM en el período 2016-2018.6
Actualmente el CGM ofrece información completa acerca de los niveles de glucosa durante todo el día, identificando la variabilidad de la glucosa, tiempos en hiperglucemia, tiempo y frecuencia de las hipoglucemias, que pasan desapercibidos por la A1c y el AMG.
Con la utilización del CGM se han establecido nuevas métricas que acompañan a la A1c en la evaluación del control glucémico. Actualmente las asociaciones científicas internacionales han tomado posición con respecto al uso del CGM y estimulan al clínico a adquirir las destrezas en la interpretación y uso racional de estas tecnologías.
¿Cómo funcionan los sistemas de Monitoreo Continuo de Glucosa?
Esquemáticamente los componentes de un CGM son:
- Un sensor
- Un transmisor
- Un receptor o dispositivo de visualización
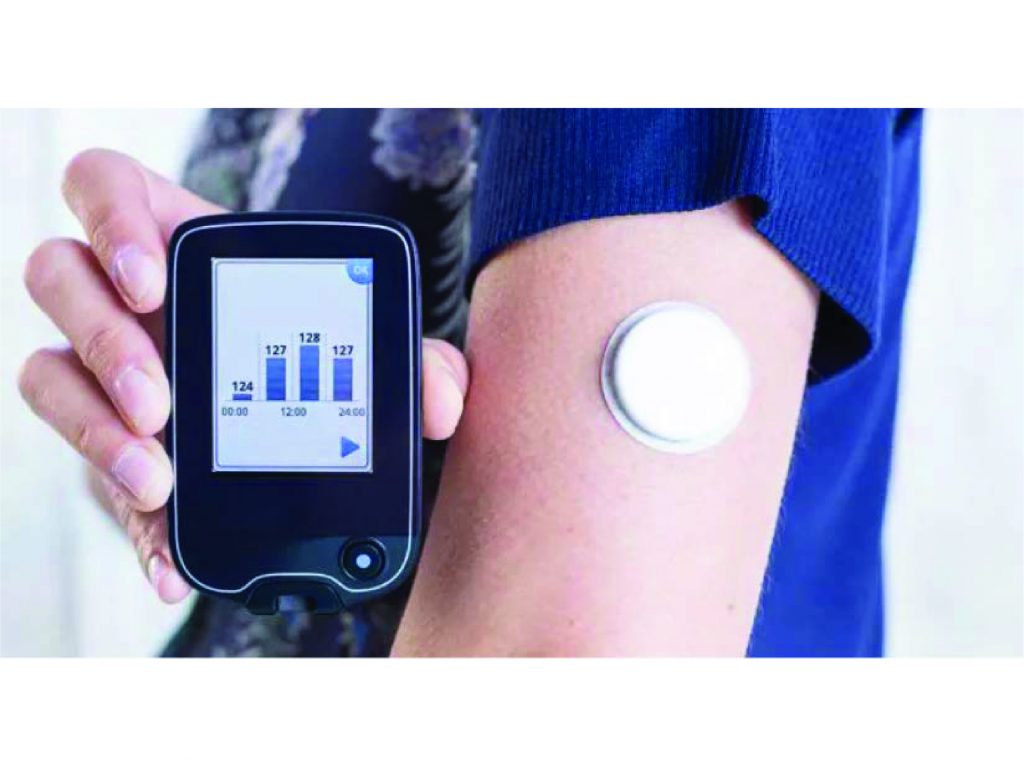
Sensor: tras su inserción a través de la piel el componente esencial es un filamento que mide la glucosa del fluido intersticial cada uno a cinco minutos.
Transmisor: cuando se ajusta al sensor puede guardar las determinaciones de glucosa o transmitirlas de forma inalámbrica al receptor o dispositivo de visualización. La información se guarda y/o transmite al receptor o dispositivo de visualización cada cinco a quince minutos.
Receptor o dispositivo de visualización: el receptor traduce los datos del transmisor que pueden ser datos almacenados (informe retrospectivo) y/o visualizados de forma intermitente o en tiempo real. En algunos casos este receptor es un dispositivo y en otros está integrado a sistemas de infusión continua de insulina (SICI).
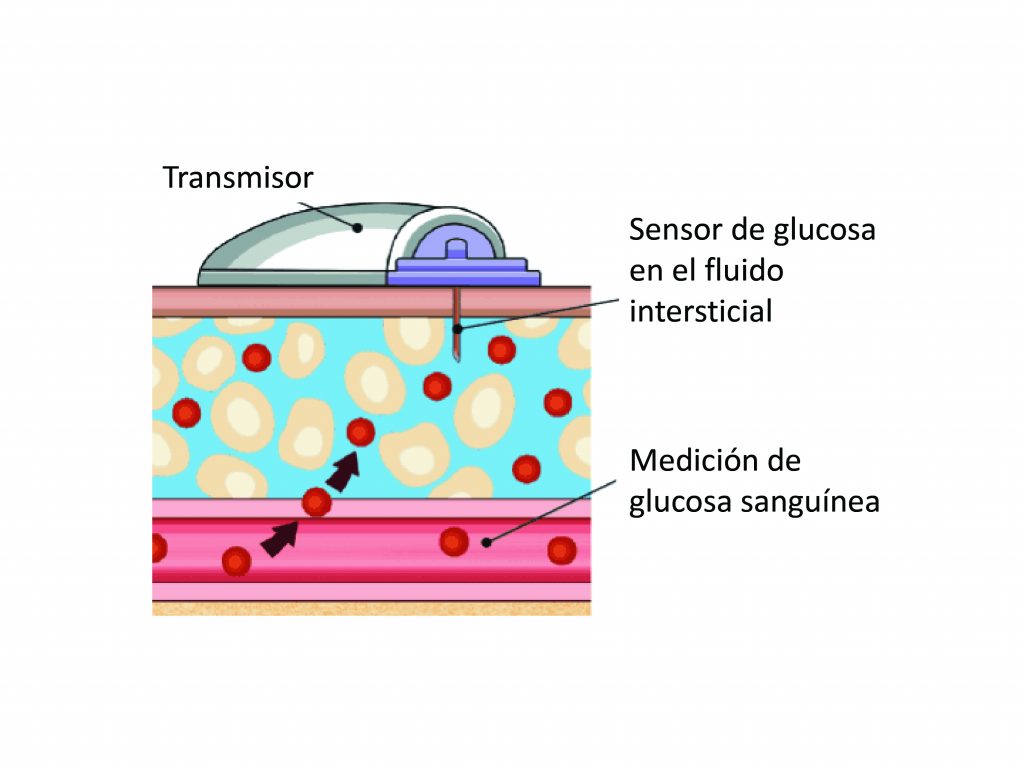
En la figura 1 se esquematiza la forma de medición de la glucosa de los CGM, observándose el sensor unido a su transmisor.
¿Con qué CGM se cuenta en la actualidad y cómo se clasifican?
En este artículo se hará referencia exclusivamente a los CGM no integrados de fábrica a los SICI.
Con fines prácticos los CGM actuales se pueden clasificar según la temporalidad de los datos ofrecidos en:
- Retrospectivos – CGM blindado o ciego: i-Pro2® (disponible en Uruguay).7
- Tiempo de monitoreo: durante seis días mide los niveles de glucosa cada cinco minutos (288 determinaciones por día).
- Es necesaria la calibración (control con glucemia capilar) dos a tres veces por día.
- Se descargan los datos y se analizan retrospectivamente para la toma de decisiones de forma prospectiva.
- Prospectivos: existen dos métodos, intermitentes (o flash) y en tiempo real o continuos
- Intermitente: Free Style Libre® (disponible en Uruguay).8,9
- Muestra el valor actual solo cuando se escanea el sensor con el dispositivo de visualización.
- El dispositivo de visualización informa el valor actual y las flechas de tendencia. Las flechas de tendencia muestran la velocidad y la dirección del cambio en el nivel de glucosa que viene sucediendo.
- Calibrado de fábrica por lo que no es necesario calibrar con digito punción.
- El transmisor almacena los datos por un período de ocho horas, por lo que es necesario escanear al menos tres veces día, esto lo define como intermitente o flash.
- Los dispositivos de visualización almacenan los datos de 90 días permitiendo un análisis preciso de todas las excursiones glucémicas en ese período.
- Es posible la descarga de datos y generación de informes a través de una plataforma web diseñada para el dispositivo.10 (https://www2.libreview.com/).
- En tiempo real o continuos: Dexcom G6® (no disponible en Uruguay).11
- Mide los niveles de glucosa cada cinco minutos (288 veces por día) y los muestra inmediatamente en el dispositivo de visualización. No es necesario el escaneo.
- El dispositivo de visualización informa el valor actual y las flechas de tendencia. Las flechas de tendencia muestran la velocidad y la dirección del cambio en el nivel de glucosa que viene sucediendo.
- Calibrado de fábrica por lo que no es necesario calibrar con digito punción.
- Dispone de alarmas que advierten al usuario cuando la glucosa se eleva o desciende por fuera del rango objetivo.
- Los datos se pueden compartir en tiempo real con teléfonos inteligentes, relojes inteligentes y vía web en forma instantánea (https://clarity.dexcom.com/).
Las principales características diferenciales de los CGM disponibles se ilustran en la figura 2.
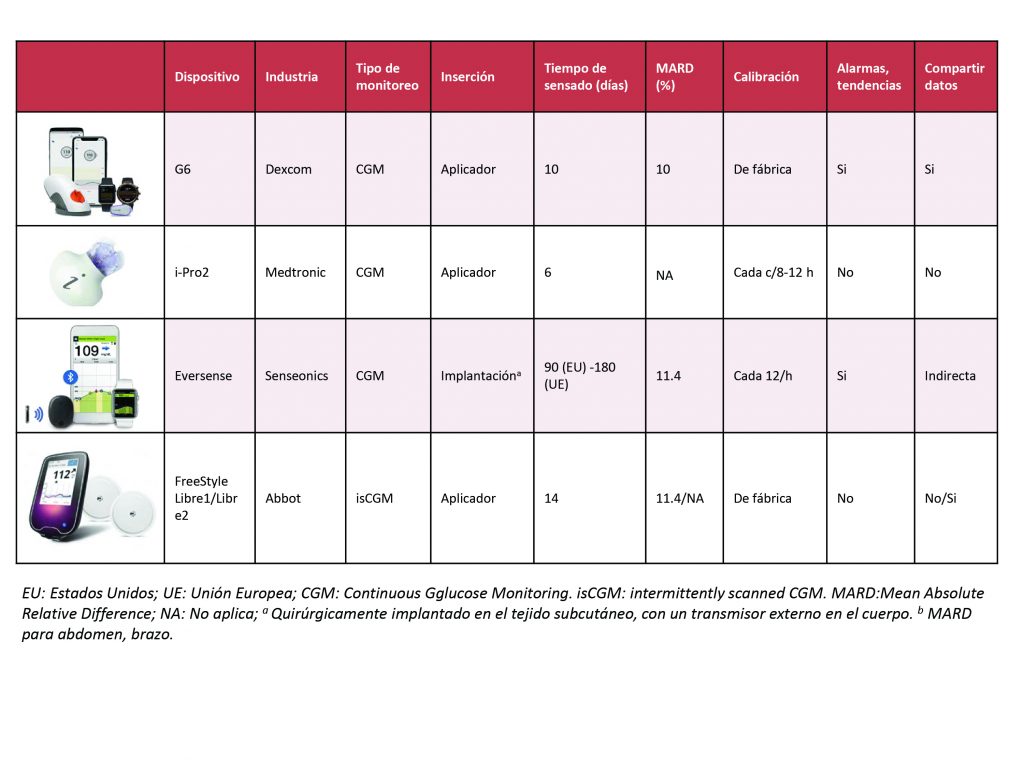
Una de las principales diferencias entre los CGM es la necesidad de calibración. Mientras que Dexcom G6® y Free Style Libre® se encuentran calibrados de fábrica, tanto Eversense como i-Pro2 requieren glucemia capilar cada ocho a doce horas para calibración.
La exactitud y precisión de los métodos de control de glucosa es fundamental para la toma de decisiones terapéuticas.
¿Cuán exactos son los sistemas de CGM?
La exactitud y precisión de los métodos de control de glucosa es fundamental para la toma de decisiones terapéuticas. El valor de referencia en la actualidad es la glucemia venosa determinada porl laboratorio. La glucemia capilar determinada por AMG debe tener una dispersión no mayor a la establecida por las normas ISO 15197:2015.
Básicamente esta norma establece como aceptable hasta 15% de diferencia entre la glucemia capilar (determinada por glucómetro) y la glucemia venosa para valores de glucemia mayores de 100 mg/dl; y para valores menores de 100 mg/dl se considera aceptable una diferencia de 15 mg/dl. 12
Los CGM no se rigen por las normas ISO, utilizando para evaluar su exactitud y precisión parámetros alternativos como el MARD, por su sigla en inglés (Mean Absolute Relative Difference).
El MARD expresa la diferencia entre el valor obtenido por el sistema de CGM y la glucemia venosa. Se ha considerado como aceptable un MARD de 10% o menor, de acuerdo a la conferencia anual de Advance Technologies and Treatments for Diabetes realizada en 2017 (ATTD 2017).
En la tabla 2 se observan las diferencias del MARD de los CGM disponibles.
¿Qué diferencias existe entre la medición de los niveles por CGM respecto a la glucemia capilar?
Habitualmente existe buena correlación entre los valores de glucosa intersticial y capilar. Sin embargo se identifica un retraso “time lag”, definido como la diferencia temporal del valor de glucemia capilar e intersticial. 13 En condiciones de estabilidad de los niveles de glucosa este tiempo es tan solo de cinco minutos.
Se debe tener en cuenta que cambios rápidos en los niveles de glucemia (tanto hiperglucemia como hipoglucemias), incrementan esta diferencia, pudiendo ser mayores a 10 minutos. Esto ocurre típicamente en los tiempos postprandiales o durante la realización de ejercicio físico.6 En estos casos se recomienda realizar glucemia capilar para contar con un nivel de glucosa confiable y actuar en consecuencia.
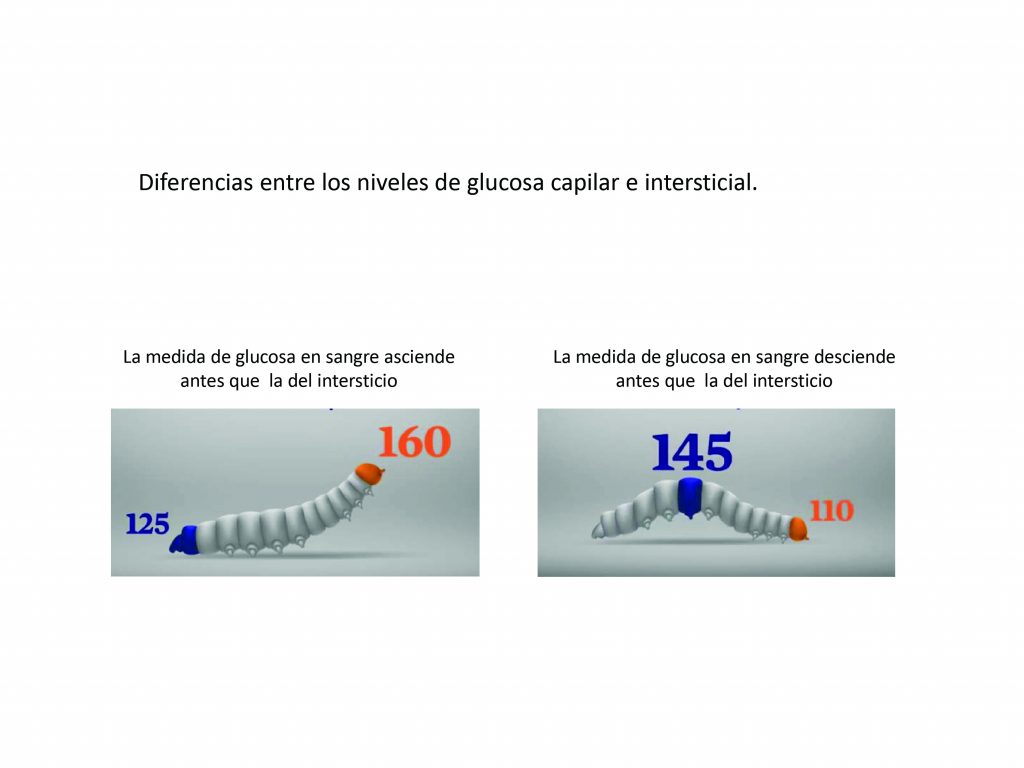
De modo gráfico, si las oscilaciones de la glucosa durante el día se compararan con los movimientos de una oruga, los primeros filamentos del cuerpo de la oruga corresponderían a la glucemia capilar y los últimos a la intersticial. En la figura 3 se observa que cuando los niveles de glucosa capilar comienzan a incrementarse, en el intersticio aún no se observa el cambio. Lo mismo ocurre ante descensos del nivel de glucosa.
¿Cómo se interpretan los datos de un CGM?
La Sociedad Americana de Diabetes (American Diabetes Association: ADA) y la Sociedad Americana de Endocrinólogos Clínicos (AACE: American Association of Clinical Endocrinologists) han publicado guías que especifican las recomendaciones para el uso de CGM en pacientes con diabetes mellitus tipo 1 y 2 (DM1 y DM2).3,14
Se cuenta además con recomendaciones de un grupo de expertos de Argentina que definen de forma clara la utilidad e indicaciones para el uso de CGM.15 En la guía de la ADA 2019, se brindan lineamientos para la interpretación de los informes de CGM, estableciendo parámetros que orientan al médico clínico. Se establece la lectura sistemática y adecuada del informe obtenido de los CGMs, en un paso a paso.14
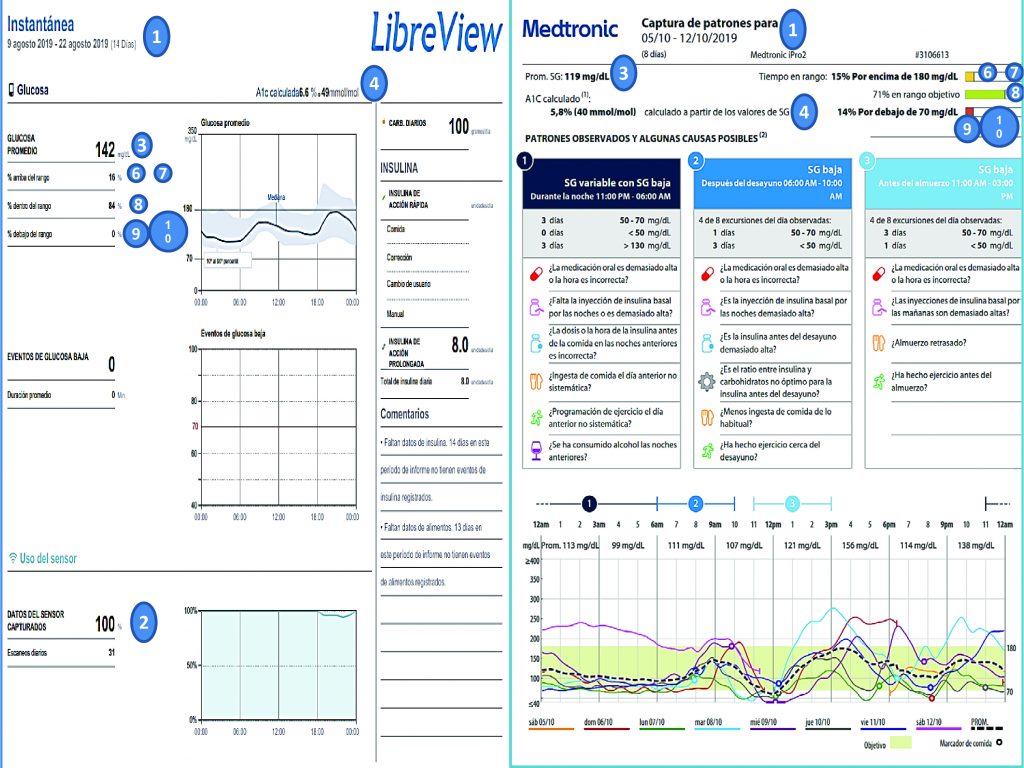
En este documento se describen 10 pasos fundamentales a reconocer en el informe:
- Número de días de uso de CGM (se recomiendan 14 días).
- Porcentaje de tiempo que CGM está activo (se recomienda el 70% de los datos de 14 días).
- Glucosa media.
- Indicador de gestión de glucosa (GMI) o A1c calculada para los días de medición.
- Coeficiente de variabilidad (CV) ≤36%.
- Tiempo por encima del rango (TAR):% de lecturas y tiempo> 250 mg/dl – Nivel 2
- Tiempo por encima del rango (TAR):% de lecturas y tiempo 181–250 mg/dl – Nivel 1
- Tiempo en rango (TIR):% de lecturas y tiempo 70–180 mg/dl – En el rango
- Tiempo por debajo del rango (TBR):% de lecturas y tiempo 54–69 mg/dl – Nivel 1
- Tiempo por debajo del rango (TBR):% de lecturas y tiempo <54 mg/dl – Nivel 2
En la figura 4 se ilustran las metas de porcentajes de Tiempos en rango de acuerdo a los criterios referidos en los pasos 6 a 10.
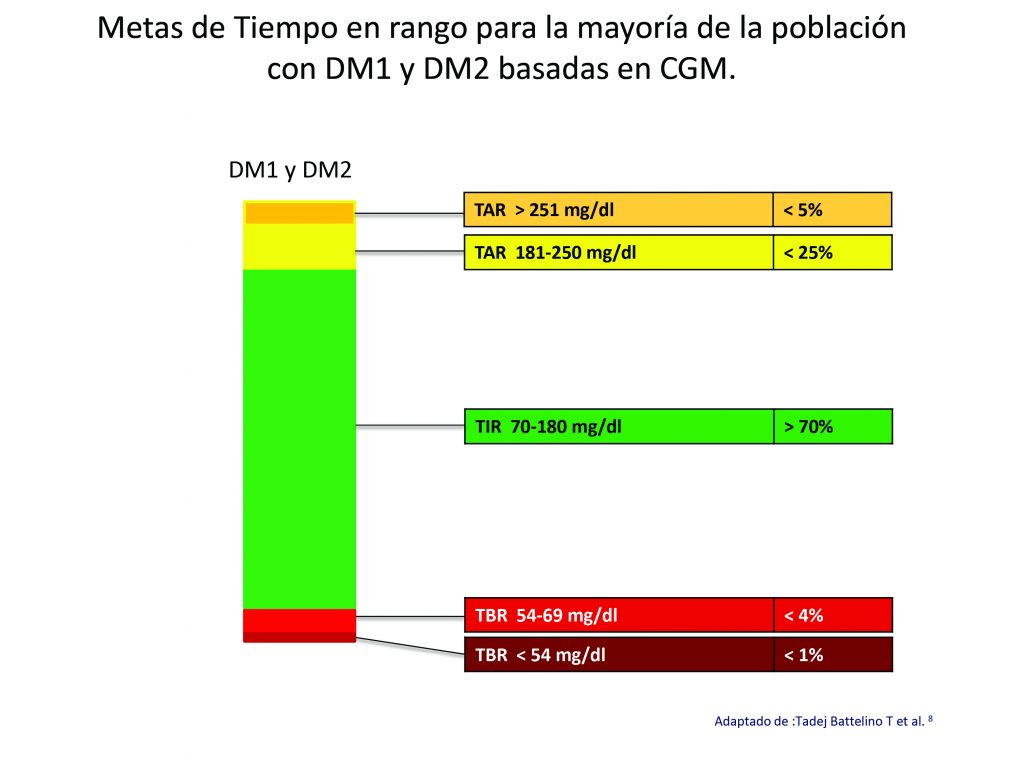
Para poblaciones de mayor riesgo como embarazadas o adulto mayor, las metas de tiempo varían, siendo mas estrictas en caso de diabetes y embarazo y mas laxas en el adulto mayor.
A continuación, se presenta un ejemplo de un registro iPro y FreeStyle Libre para identificar los pasos a seguir en la lectura (Figura 5).
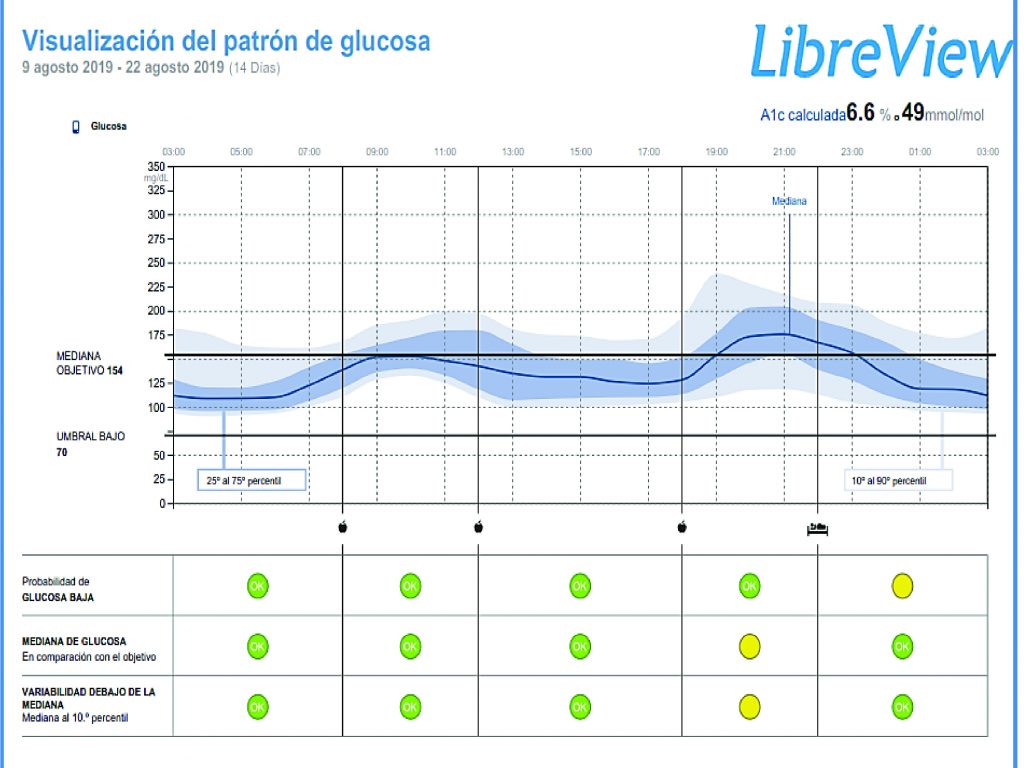
Además de los datos estadísticos y metas referidas, el informe de CGM ofrece un perfil ambulatorio de la glucosa – AGP por su sigla en inglés (Ambulatory Glucose Profile), o visualización del patrón de glucosa, que representa la sumatoria de los valores de glucosa del período analizado, con la marcación de la mediana (50%) y otros percentiles que se observen en un día en particular, como se observa en la figura 6.
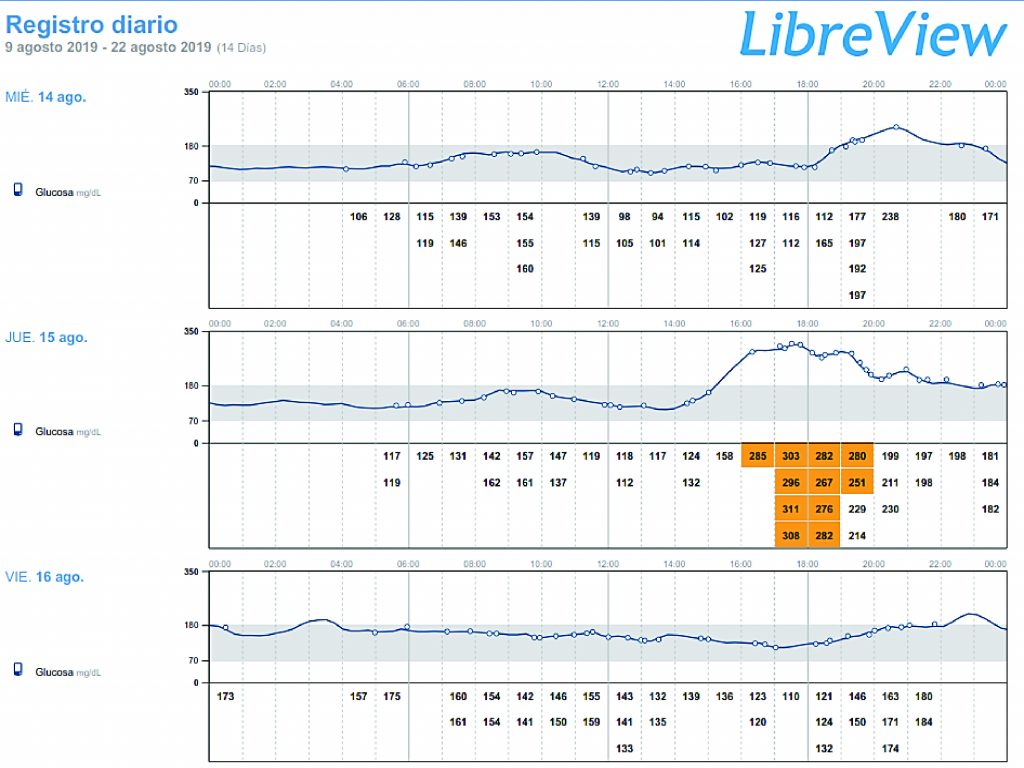
Finalmente, en el registro diario, se puede observar monitoreo de la glucosa día a día, las oscilaciones, las hipoglucemias, los periodos nocturnos, diurnos y el promedio de glucosa diario, entre otros. Ver figura 7.
¿Qué beneficios clínicos tiene el uso de CGM?
Desde su primera mención publicada hasta la actualidad, existen más de 5.000 publicaciones relacionadas al CGM. El primer gran estudio randomizado controlado (ERC) con CGM fue realizado por la Juvenil Diabetes Research Foundation (JDRF) y demostró que su uso fue eficaz para reducir los niveles de A1c y las hipoglucemias en adultos. 17
Posteriormente se han evidenciado los beneficios clínicos en pacientes con hipoglucemias severas o inadvertidas 18-20 , el logro de metas A1c evitando las excursiones e incrementando la calidad de vida de los pacientes.21.22
El uso de CGM ha permitido un rol más protagónico del paciente, que al obtener datos de su nivel de glucosa en tiempo real es capaz de tomar decisiones en cuanto a su plan de alimentación, ejercicio o correcciones con bolos de insulina, y fundamentalmente, reaccionar de forma inmediata para evitar o reducir la aparición de hipoglucemias en pacientes niños, adolescentes y adultos 23-25.
Las herramientas digitales de descarga de datos de los CGMs, permiten el análisis retrospectivo, identificando áreas problemáticas y determinando de forma individualizada las metas glucémicas a alcanzar. 26
Estos beneficios se evidencian en pacientes con dosis múltiples de insulina o SICI.27
Recientemente el estudio COMISAIR 28, ha demostrado que el beneficio clínico del paciente recae en el CGM independientemente del uso de dosis múltiples o SICI, generando atención especial en el aprendizaje de los CGMs en la práctica clínica.
La indicación de CGM aporta beneficios para tomar conductas terapéuticas por parte del equipo de salud y del paciente, integrando el trabajo en equipo. 10
¿En qué pacientes con diabetes indicar CGM?
Existe un crecimiento exponencial en el uso de CGM en todos los grupos de pacientes.29
A modo de resumen y basados en los beneficios del uso de CGM, los autores de este artículo recomiendan:
- Paciente con DM1
- Paciente con DM2 tratados con isulina
- Pacientes con alto riesgo de hipoglucemia (tratados con sulfonilureas, adulto mayor o con comorbilidades como enfermedad renal crónica).
- Diabetes gestacional
Una vez seleccionados, los pacientes con CGM deben recibir educación y entrenamiento para un uso adecuado y una interpretación correcta de los datos proporcionados.
Conclusiones
La inclusión de las tecnologías aplicadas a la diabetes, específicamente los CGMs, han revolucionado la forma de afrontar el tratamiento de los pacientes, permitiendo una mayor comprensión del comportamiento de la enfermedad tanto para el médico como para el paciente.
El tiempo en rango recomendado de 70%, equivalente a aproximadamente 17 horas al día, permite al médico tener un objetivo temporal en 24 horas, con niveles de glucosa entre 70-180mg/dl limitando la variabilidad, pudiendo realizar un análisis de la realidad mas exacto que mediante el uso de AMG.
La posibilidad en la práctica clínica de evaluar la respuesta farmacológica, número de hipoglucemias, tiempo en hipoglucemias, tiempo en hiperglucemias, horarios de evento, la adherencia al ejercicio y alimentación, se ha convertido en un reto que debe generar acciones para el cambio al momento de realizar las indicaciones terapéuticas.
El paciente, quien al tener la posibilidad de observar el comportamiento de su glucosa, es tomador de decisiones, acompañado e interactuando con el médico en la individualización del tratamiento.
Los múltiples canales digitales de conectividad de los equipos, permiten hacer partícipes en tiempo real al paciente, médicos, cuidadores y/o familiares.
Los CGMs a nivel mundial se han convertido en un aliado estratégico en la identificación de problemas relacionados al comportamiento de la glucosa, incrementando la precisión del control y mejorando la calidad de vida.
Persisten aún pendientes retos y limitaciones de los CGMs que se deben conocer, como el “time lag”, las diferencias entre glucemia capilar e intersticial y la precisión. Estos retos no están ajenos a los avances tecnológicos que se perfeccionan día a día.
Finalmente, al tener la gran oportunidad de contar con CGMs en el país, es necesario optimizar la educación del equipo de salud y de los pacientes con diabetes, para el uso mas eficiente de este recurso.
Referencias bibliográficas
- Shrom, D., Sarwat, S., Ilag, L. and Bloomgarden, Z.T. (2010), Does A1c consistently reflect mean plasma glucose? Journal of Diabetes, 2: 92-96. doi:10.1111/j.1753-0407.2010.00066.x.
- Ajjan RA. How Can We Realize the Clinical Benefits of Continuous Glucose Monitoring? Diabetes Technol Ther. 2017; 19(S2):S27–S36. doi:10.1089/dia.2017.0021.
- Fonseca VA, Grunberg G, Anhalt H et al. Continuous glucose monitoring: a consensus conference of the American Associatios of Clinical Endocrinologists and American College of Endocrinology. Endocr Pract 2016; 22(8):1008-1021.
- Pfützner A, Weissmann J, Mougiakakou S, Daskalaki E, Weis N, Ziegler R. Glycemic Variability Is Associated with Frequency of Blood Glucose Testing and Bolus: Post Hoc Analysis Results from the ProAct Study. Diabetes Technol Ther. 2015; 17(6):392–397.
- Miller KM, Beck RW, Bergenstal RM, et al. Evidence of a strong association between frequency of self-monitoring of blood glucose and hemoglobin A1c levels in T1D exchange clinic registry participants. Diabetes Care. 2013; 36:2009–2014.
- Foster NC, Beck RW, Miller KM, et al. State of type 1 diabetes management and outcomes from the T1D exchange in 2016-2018. Diabetes Technol Ther 2019; 21(2):66–72.
- https://professional.medtronicdiabetes.com/ipro2-professional-cgm
- Freestyle Libre reader. 2018. Available from https://www.freestylelibre.co.uk/libre/products/reader.html Accessed May 2019. Abbott.
- Freestyle Libre sensor. 2018. Available from https://www.freestylelibre.co.uk/libre/products/sensors.html Accessed May 2019.
- Dovc K, Battelino T. Evolution of Diabetes Technology. Endocrinol Metab Clin N Am 49; 2020: 1-18.
- Dexcom. What is (CGM) Continuous Glucose Monitoring? Available from https://www.dexcom.com/continuous-glucose-monitoring Accessed May 2019.
- Jendrike, N., Baumstark, A., Kamecke, U., Haug, C., & Freckmann, G. (2017). ISO 15197: 2013 Evaluation of a Blood Glucose Monitoring System’s Measurement Accuracy. Journal of Diabetes Science and Technology, 11(6), 1275–1276.doi:10.1177/1932296817727550.
- Scuffi C, Lucarelli F, Valgimigli F. Minimizing the impact of time lag variability on accuracy evaluation of continuous glucose monitoring systems. J Diabetes Sci Technol. 2012; (6):1383–1391. Published 2012 Nov 1. doi:10.1177/193229681200600618
- American Diabetes Association. Standards of medical care in diabetes, 2018, Diabetes Care 2018; 41(Suppl.1):S126-S133.
- Litwak L, Querzoli I, Musso C et al. Monitoreo continuo de glucosa. Utilidades e indicaciones. MEDICINA (Buenos Aires) 2019; 79:44-52.
- Battelino T, Danne T, Bergenstal et al. Clinical Targets for Continuous Glucose Monitoring Data. Interpretation: Recomendations From the International Consensus Time in Range. Diabetes Care 2019; 42:1593-1603.
- The Juvenile Diabetes Research Foundation Continuous Glucose Monitoring Study Group*. Continuous glucose monitoring and intensive treatment of type 1 diabetes. N Engl J Med 2008;359(14):1464–76
- Bergenstal RM. Continuous glucose monitoring: transforming diabetes management step by step. Lancet 2018; 391(10128):1334–6.
- Little SA, Speight J, Leelarathna L, et al. Sustained reduction in severe hypoglycemia in adults with type 1 diabetes complicated by impaired awareness of hypoglycemia: two-year follow-up in the HypoCOMPaSS randomized clinical Trial. Diabetes Care 2018; 41(8):1600–7.
- Heinemann L, Freckmann G, Ehrmann D, et al. Real-time continuous glucose monitoring in adults with type 1 diabetes and impaired hypoglycaemia awareness or severe hypoglycaemia treated with multiple daily insulin injections (HypoDE): a multicentre, randomised controlled trial. Lancet 2018. https://doi.org/ 10.1016/S0140-6736(18)30297-6.
- Polonsky WH, Hessler D, Ruedy KJ, et al. The impact of continuous glucose monitoring on markers of quality of life in adults with type 1 diabetes: further findings from the DIAMOND randomized clinical trial. Diabetes Care 2017; 40(6):736–41.
- Hilliard ME, Levy W, Anderson BJ, et al. Benefits and barriers of continuous glucose monitoring in young children with type 1 diabetes. Diabetes Technol Ther 2019; 21(9):493–8.
- Aleppo G, Laffel LM, Ahmann AJ, et al. A practical approach to using trend arrows on the Dexcom G5 CGM system for the management of adults with diabetes. J Endocr Soc 2017;1:1445– 1460.
- Laffel LM, Aleppo G, Buckingham BA, et al. A practical approach to using trend arrows on the Dexcom G5 CGM system to manage children and adolescents with diabetes. J Endocr Soc 2017; 1: 1461–1476. Kudva YC, Ahmann AJ, Bergenstal RM, et al. Approach to using trend arrows in the FreeStyle Libre Flash Glucose Monitoring Systems in adults. J Endocr Soc 2018; 2:1320–1337.
- Carlson AL, Mullen DM, Bergenstal RM. Clinical use of continuous glucose monitoring in adults with type 2 diabetes. Diabetes Technol Ther 2017; 19(Suppl. 2):S4–S11.
- Hirsch IB, Verderese CA. Professional flash continuous glucose monitoring with ambulatory glucose profile reporting to supplement A1C: rationale and practical implementation. Endocr Pract 2017; 23:1333–1344.
- Peters AL, Ahmann AJ, Battelino T, et al. Diabetes technology—continuous subcutaneous insulin infusion therapy and continuous glucose monitoring in adults: an Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2016; 101(11):3922–37.
- Šoupal, J., Petruželková, L., Grunberger, G., et al. (2019). Glycemic Outcomes in Adults With T1D Are Impacted More by Continuous Glucose Monitoring Than by Insulin Delivery Method: 3 Years of Follow-Up From the COMISAIR Study. Diabetes Care, dc190888.doi:10.2337/dc19-0888.
- Foster NC, Beck RW, Miller KM, et al. State of type 1 diabetes management and outcomes from the T1D exchange in 2016-2018. Diabetes Technol Ther 2019; 21(2):66–72.

Dra. Natalia Miranda
Médico Internista
Diabetóloga
Máster en Enfermedad Aterotrombótica.
Coordinadora Clínica del Posgrado de Especialización en Diabetes – Universidad Católica del Uruguay.
Vicepresidente de la Sociedad Uruguaya de Aterosclerosis.

Dr. Frank Espinoza Morales
Medico Cirujano
Especialista en Nutrición con Orientación en Obesidad.
Especializado en Diabetes. Sociedad Argentina de Diabetes.
Director de CAVIMEDIC. Lima- Perú
Centro de Atención y Tecnologías Médicas
en Diabetes.
Docente de Maestría en Diabetes y Obesidad con mención en manejo nutricional . UPCH