Las osteomielitis crónicas (OMC) frecuentemente se definen como la presencia de una infección ósea de más de 1 mes, en presencia de hueso desvitalizado. (1)
La incidencia varía en función de la localización geográfica (2) entre 10 y 25 por 100.000 niños sanos (3). Es mucho mayor en países en desarrollo, como consecuencia del diagnóstico retrasado y el tratamiento incompleto (1).
En el Centro Hospitalario Pereira Rosell (CHPR) se registran 12.4 casos al año de infecciones osteoarticulares (agudas y crónicas) variando entre 8 a 21 casos al año entre 2009 y 2015 (4). En Uruguay no hay un registro epidemiológico específico de esta patología.
Aunque la prevalencia de osteomielitis va disminuyendo, la presentación clínica ha variado a casos más complejos y por microorganismos más resistentes (5).El agente etiológico más frecuentes es el S.Aureus, pero la ecología bacteriana ha cambiado y deben investigarse nuevos gérmenes(2).
La mayoría de las infecciones son hematógenas, las siguen en frecuencia infecciones por contigüidad y menos frecuentemente luego de intervenciones quirúrgicas (5).
Se presentan con gran variabilidad clínica, se destaca el dolor crónico y fístula.
Deben monitorizarse distintos elementos paraclínicos como glóbulos blancos (GB), velocidad de eritrosedimentación (VES) y proteína C reactiva (PCR), aunque no hay un consenso de cuando debería testearse (6).
Según la clasificación de Cierny-Mader (osteomielitis de adulto) las clasificamos desde un punto de vista anatómico (1-2-3-4) y fisiológico (A-B-C) del hospedero (7). La infección crónica se clasifica como una Tipo 3 o 4 anatómica y siempre es al menos tipo B ya que el huésped tiene una patología de larga evolución por lo que se considera como comprometido (7).
El tratamiento de las infecciones crónicas siempre debe ser médico y quirúrgico y guiado por un equipo multi-disciplinario. El tratamiento antibiótico debe ser dirigido al germen y con un curso prolongado, no hay un consenso sobre la duración del mismo(8).
El tratamiento quirúrgico es complejo y debe ser planificado, generalmente en varias etapas(5). Se han descrito numerosas técnicas quirúrgicas desde simples limpiezas hasta debridamientos radicales. El cemento con antibióticos se utiliza en la técnica de Inducción de membrana de Masquelet o en perlas, logrando mejor difusión local de antibióticos. (9)
Este estudio surge debido a la falta de consenso ante esta enfermedad y la variedad de conductas quirúrgicas, analizando la presentación clínica, paraclínica y el abordaje terapéutico.
OBJETIVOS
Objetivo principal
Evaluar opciones de tratamiento quirúrgico en las osteomielitis crónicas
Objetivos secundarios
Describir distintas opciones de tratamiento quirúrgico, sus indicaciones, resultados y complicaciones
Evaluar protocolos de duración del tratamiento antibiótico
Valorar las características epidemiológicas, clínicas y paraclínicas de las OMC
MATERIALES Y METODOS
Estrategia de búsqueda
Se realizó una búsqueda bibliográfica sistematizada en las base de datos Pubmed con los siguientes criterios:
Criterios de inclusión
Humanos
Niños (filtro 0-18 años)
Fisis abierta (lectura completa)
Estudios sobre osteomielitis de los miembros torácicos o pélvicos.
Estudios que describan el tratamiento quirúrgico
Criterios de exclusión
Estudios con población mezclada niños/adultos
Estudios descriptivos microbiológicos
Estudios epidemiológicos
Síndromes asociados
Infecciones óseas del cráneo, mandíbula y el raquis
Reporte aislado de caso
RESULTADOS DE LA BUSQUEDA
La búsqueda bibliográfica inicial fue realizada en junio de 2020 y arrojó 2683 artículos con las palabras clave “chronic osteomyelitis”. Limitamos la búsqueda en los últimos 20 años (2000 a 2020) y quedaron 1319 artículos. Se seleccionaron los filtros “humanos” y “niños (0-18 años) y obtuvimos 324 artículos.
Seleccionamos 107 por título y quedamos con 35 artículos al leer el Abstract. Estos 35 artículos se leyeron de forma completa para aplicar nuevamente los criterios de inclusión y exclusión para seleccionar finalmente los 12 artículos que se analizan en esta revisión. (FIGURA 1).
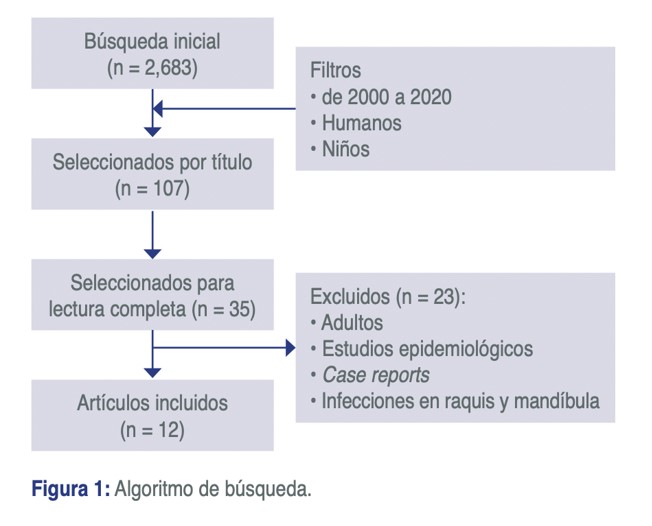
De los 12 artículos seleccionados: 11 fueron observacionales y únicamente 1 experimental.
Según el nivel de evidencia:
NE tipo III: 2 artículos
NE IV: 10 artículos
Según tipo de estudios:
Series de casos: 9.
Una Cohorte retrospectiva: 1. Dos cohortes retrospectivas: 1.
Una cohorte prospectiva: 1.
Extracción de datos:
Cantidad de pacientes. Sexo. Edad.
Clínica inicial
Topografía ósea
Etiología de la infección
Estudios imagenológica solicitados
Paraclínica inicial: Glóbulos blancos, VES y PCR
Tratamiento quirúrgico inicial. Postoperatorio. Etapas quirúrgicas siguientes
Germen y Antibioticoterapia
Resultados y conclusiones
Se extrajeron los datos aislados de cada artículo, y se elaboro una tabla de análisis de los mismos. Se realizo un análisis comparativo no analítico de las características de la población, de la presentación clínica y de los distintos tratamientos sus resultados y complicaciones.
ANALISIS DE LOS RESULTADOS
En total se analizaron 358 pacientes en los 12 artículos seleccionados. Del análisis general un 61% fue de sexo masculino, y la edad promedio fue de 8.02 años (media aritmética).
La presentación clínica inicial fue variable y difícilmente comparable. 11 artículos describían la clínica inicial siendo la fístula el elemento clínico más frecuente con más del 70% de todos los pacientes analizados. 15% presentaban signos fluctuantes locales, 9% por dolor crónico, 3% con fiebre, 1.5% con fractura patológica.
Con respecto al hueso involucrado el 89% corresponde a los miembros inferiores, siendo 48% en tibia, 34% fémur y 7% en pie. En miembros superiores 6% corresponde a OMC de humero y 4% de antebrazo. 1% están descritas como otras: pelvis, clavícula y esternón.
La etiología fue hematógena en un 72%, por contigüidad 9%, relacionada a osteosintesis 7%, secundaria a fractura expuesta en un 2%, postraumática 4%, herida local 2%, y desconocida en un 4%.
De los 358 pacientes que engloba este trabajo, en 90 no se explicita el germen actuante ni el resultado del estudio microbiológico(10).El resto expone detalladamente a que germen fue positivo y en el caso de infecciones por S.Aureus si era resistente a meticilina o no.
De los 268 pacientes, los cultivos no tuvieron desarrollo en 65 (24.2%).
De los cultivos positivos tenemos que la gran mayoría pertenecen a S.Aureus con el 72.4%. Al analizarlos por separado, el 39.4% fue a SAMAR.
Un 12.8% correspondió a Gram negativos (Enterococos, E.Choli, Pseudomonas, Salmonella, Proteus), y un 9.8% a Estreptococos spp. (B Hemolítico, Pyogenes, Viridans) (FIGURA 2).
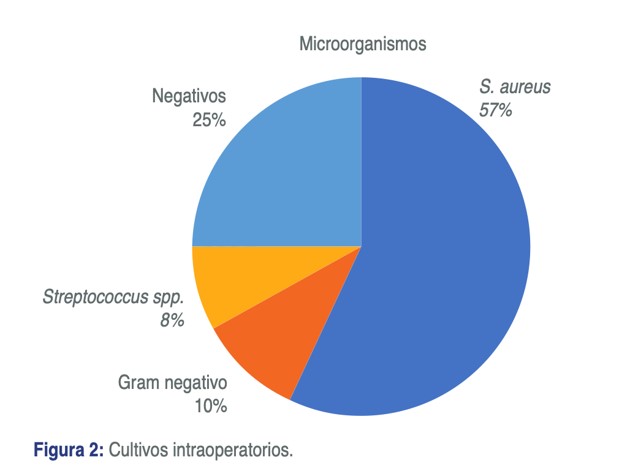
El 22% de los pacientes presentó cultivos polimicrobianos.
Analizando la paraclínica, no todos los autores la mencionan. Solicitan hemograma, valorando principalmente GB y el perfil de neutrófilos, VES y PCR.
Aunque no se realizó un análisis estadístico estricto, al separar los valores específicos de cada parámetro, en cada paciente, resulta que:
- los GB tienen un promedio en normal y un 10-80% de los pacientes lo presentan elevado.
- la PCR tiene un promedio de 23 (1.44-66.4) y 10-80% de los pacientes lo presentan elevado.
- la VES tiene un promedio de 51.3 (23.8-86.6 mm/h) y entre 50-100% de los pacientes lo presentan elevado.
Consideramos valores alterados como: GB>14×103 , VES>20mm3/h, PCR>20 ya que es indicativo de infección bacteriana(11). (FIGURA 3)
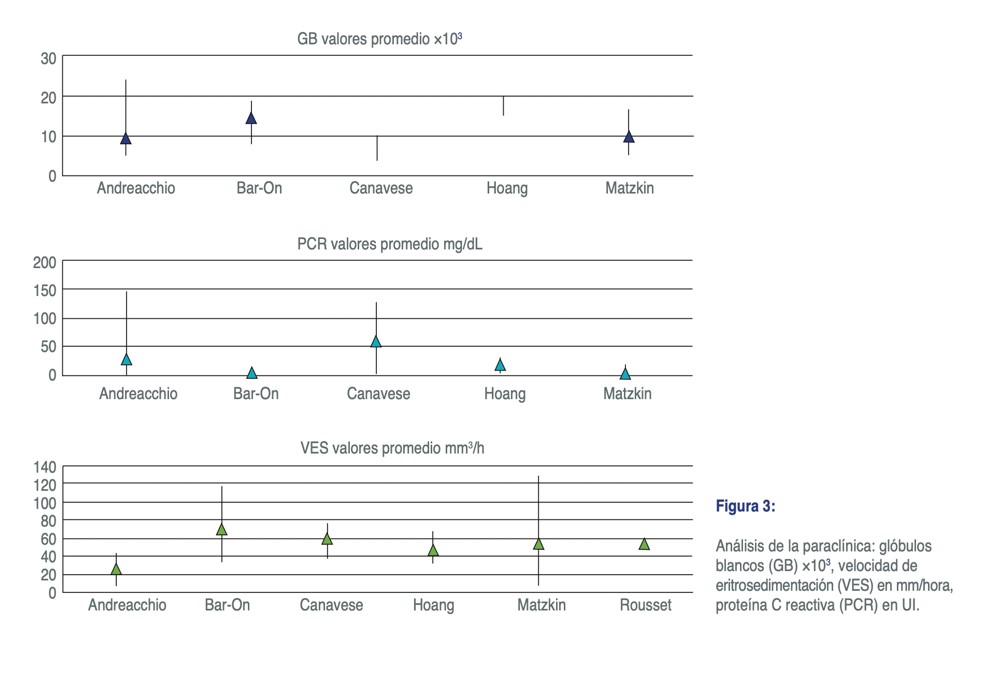
La duración del tratamiento antibiótico se expuso en tablas, no se realizó un análisis estadístico por la variabilidad de estudios. El tratamiento intravenoso inicial duró un promedio de 3,5 semanas (máximo de 13 semanas) y siguiendo con vía oral por 7,4 semanas (máximo de 24 semanas).
Los autores realizan el paso del tratamiento intravenoso a vía oral con la mejoría clínica y paraclínica, y varía en cada paciente.
TECNICA QUIRURGICA Y RESULTADOS
Se utilizaron distintas técnicas quirúrgicas. Todos los trabajos implican cirugía en 1 o más etapas. Siempre la etapa inicial implica limpieza quirúrgica y debridamiento de tejido necrótico.
Los procedimientos de desbridamiento fueron 3: corticotomía, fresado del canal, necrectomía amplia hasta hueso sano. Se realizó secuestrectomía y fistulectomía en caso de presentar secuestro o fistula. 1 único paciente requirió una amputación inicial (19).
Solo 2 autores realizaron su procedimiento en 1 único acto quirúrgico, el resto realizaron varias etapas según la necesidad de cada paciente, con un variable entre 2-8 cirugías.
Se analizan por separado según técnica quirúrgica.
Limpiezas seriadas:
Bar-On etal, Matzkin etal y Mantero etal analizan 4, 96 y 55 pacientes respectivamente a los que se le realiza debridamiento extenso, fresado e irrigación como conducta quirúrgica, sin asociar procedimientos de reconstrucción.
Bar-on agrega cemento con antibiótico y lo fija con clavillos de Krischner (CK) o Steinman. En una 2da etapa quirúrgica retira el cemento y realiza un nuevo fresado del canal.
Mantero realiza el trabajo más completo y con mayor nivel de evidencia al seguir una cohorte de pacientes tratados con un mismo método. Luego de la limpieza inicial los pacientes quedan con un lavado continuo del canal medular con el método IN-OUT por 7 días. Bar-on también usa este método en 2 pacientes.
De las complicaciones destacan: absceso local, defecto de partes blandas que requirió sistema de succión negativa (VAC), refractura y consolidación viciosa que requirió fijadores externos (FE). Concluyen que es una patología de tratamiento complejo y es necesario tratamiento quirúrgico agresivo más antibióticos. Respecto al lavado In-Out los resultados mostraron un 87.5% de curación al final del seguimiento (1-84 meses).
Masquelet (o Inducción de membrana):
Canavese etal, Felden etal y Rousset etal realizan esta técnica, siguiendo 5, 3 y 8 pacientes respectivamente. Este procedimiento requiere un debridamiento inicial, uso de espaciador con cemento y luego una 2ª cirugía de reconstrucción retirando el cemento y rellenando con injerto óseo.
Se utiliza osteosíntesis para fijar el cemento con CK o Steinman intramedular según el paciente y el defecto óseo.
Rousset etal realiza una comparación retrospectiva entre 2 cohortes utilizando autoinjerto y sustituto óseo y concluye que los pacientes con sustituto óseo consolidaron antes que los autoinjertos aunque afirman que son necesarios estudios más amplios y con defectos óseos mayores.
Los autores realizan la 2ª cirugía luego de la normalización de parámetros infecciosos.
Otros procedimientos de reconstrucción:
Fueron variados, se destacan: osteogénesis por distracción (Ilizarov), transferencia de Huntington, transferencia de peroné, relleno con musculo.
Andreacchio etal es el único autor de esta revisión que realiza su procedimiento en una única etapa. Se retira el hueso desvitalizado y se rellena con sustituto óseo de sulfato de calcio con Tobramicina. Tuvo muy buena evolución de sus pacientes, sin complicaciones y un 100% de efectividad en el tratamiento contra la infección combinado con los antibióticos. Tiene como ventaja principal que es única cirugía, no hay necesidad de retiro del injerto y reduce estadía hospitalaria.
Hoang etal realiza un procedimiento original en el que se rellena el defecto óseo con injerto muscular. El procedimiento consiste en el uso de musculo Recto interno vascularizado (de miembro contralateral), anastomosando a arteria tibial posterior, rellenando el defecto óseo y realizando cobertura local con injerto de piel libre. Siguieron 6 pacientes con 100% efectividad, sin recidivas a los 3 años seguimiento. En caso de corticotomía mas amplia recomiendan asociar FE.
Shretha etal sigue a 90 pacientes para identificar problemas en el manejo de esta patología, tratados con diversas técnicas. En el 31% realizaron algún procedimiento aparte de la necrectomía inicial: fijación interna (CK, o placas), injerto de peroné, transferencia de Huntington, FE, reconstrucción con Ilizarov y amputación. Los fallos en las cirugías iniciales y las complicaciones como no-unión y dismetrías se convirtieron a Técnica de Ilizarov. En las conclusiones destacan la diversidad de procedimientos y la alta tasa de complicaciones. Recomiendan uso de Ilizarov para el tratamiento de la nounión y el acortamiento.
Unal etal sigue a 22 pacientes de forma retrospectiva a los que realiza procedimientos variables, pero siempre en una primera etapa realiza debridamiento. 59% solo requirió debridamiento y antibióticos, el resto: injerto óseo, osteogénesis por distracción con fijadores monoplanares, transferencia de Huntington. Realizaron yeso o fijación externa dependiendo del contacto cortical (al menos 2 corticales). Destacan la importancia del involucro como factor protector. Como complicaciones tuvieron defectos segmentarios en el 40%, angulaciones 18%, no unión 1 caso.
Concluyen que la mayoría de los pacientes tienen más de 1 cirugía y más de 1 complicación. El tratamiento debe dirigirse además de la infección a tratar sus complicaciones. El involucro ayuda a preservar la longitud y regeneración ósea.
Wirbel etal sigue a 27 pacientes de los que solo 4 requirieron reconstrucción utilizando transplantes óseos. Como complicaciones reportan un 48% de restricciones funcionales, 22% de dismetrías. 4 requirieron artrodesis.
En caso de defectos de partes blandas utilizaron VAC inicialmente y luego injerto por Cirugía Plástica.
Concluyen que los paises subdesarrollados tienen formas más graves y evolucionadas y que el debridamiento óseo radical es el aspecto más importante del tratamiento. Los procedimientos de reconstrucción varían según sector y tamaño del defecto.
Yeargan etal sigue 30 pacientes con tratamientos variables, el 80% solo requirió debridamientos. La reconstrucción fue variable: sinostosis tibio-peronea en 4, Ilizarov en 5, procedimientos de partes blandas en 10. De las complicaciones se destacan recurrencia en 4, no-union en 3, dismetría en 3, fracturas en 3. Concluyen que la cronicidad implica un abordaje más agresivo que requeriría procedimientos de reconstrucción luego. Se recomienda Ilizarov para manejar dismetrías y angulaciones.
DISCUSIÓN
La fístula se presenta como el síntoma principal en los artículos más grandes de esta revisión (12,13). Esto se explicaría debido a un diagnóstico retrasado y asociado a una mala conducta terapéutica inicial, especialmente en países subdesarrollados (Hawaii, Kenia, Nepal). La fiebre es un signo muy poco frecuente a diferencia de las Osteomielitis Agudas. De acuerdo con algunos autores el 50% se presenta con síntomas vagos, como dolor, edema local y en pocos casos fiebre(6).
En nuestra revisión tuvimos que un 89% de los pacientes presentaba compromiso de los miembros inferiores. El hueso más frecuentemente involucrado es la tibia seguido por el fémur y el humero, coincidiendo con la bibliografía(1).
La etiología es en su mayoría hematógena (72%) y es secundaria a osteomielitis hematógena aguda (OHA) no resueltas por tratamiento inefectivo o antibioticoterapia insuficiente, como ya habíamos dicho. Un 24% de las OMC fueron secundarios a traumatismos, heridas e infecciones por contigüidad, sabiendo que la puerta de entrada puede ser cercana o alejada al foco de OMC.
Es importante realizar una valoración inicial destacando GB, VES y PCR. Estos pueden presentarse elevados o en rango normal. La normalidad de los mismos no excluye la infección al ser un proceso crónico. Los valores fueron muy diversos en los 3 parámetros, ninguno de ellos por si solo permite confirmar o excluir la enfermedad.
La VES por lo general esta elevada ya que es un parámetro inflamatorio.
La PCR indica actividad del proceso infeccioso y es el parámetro evolutivo más fiel(1,6), por lo que una PCR en descenso indicaría buena respuesta al tratamiento y una PCR en ascenso, lo opuesto.
Un trabajo mexicano del 2000 reporta que la VES se elevo en un 61%, y la leucocitosis en un 46% valores que por sí solos son poco útiles para el diagnostico inicial (14).
Los autores utilizan los parámetros infecciosos no como diagnóstico sino para definir la etapa de la conducta terapéutica, especialmente en el caso de realizar un procedimiento de Inducción de membrana. Los parámetros infecciosos en descenso (luego de la necrectomía y antibioticoterapia IV) definen el momento de realizar el retiro de cemento y la colocación de injerto óseo(15–18) así como también el paso de tratamiento intravenoso a vía oral.
Un detalle es que los pacientes con una fistula activa(12,13) se presentan clínicamente sin fiebre y con parámetros infecciosos en rango normal.
S.Aureus es el organismo causante más común en las OMC(1–6,11).
En un trabajo retrospectivo del Hospital Pereira Rosell se analizaron todos los pacientes con infecciones osteoarticulares entre 2009-2015. Se aislaron microorganismos en un 34% de los pacientes en tejido óseo, articular o hemocultivos. De estos el 70% cultivó S.Aureus, y el 13% fue resistente a meticilina. 5% fueron polimicrobianos(4).
No se sabe porque los cultivos tienen tan poco rendimiento. En series extranjeras, la frecuencia de detección etiológica no supera el 50%(19) .
En nuestra revisión un 75% de los cultivos fueron positivos y de estos el 72.4% a S.Aureus con un 39.4% resistente a meticilina. Además 22% fueron polimicrobianos. Valores bastante distintos a los trabajos locales e internacionales, no pudiendo concluir cuales son los factores que mejoran el rendimiento de los cultivos.
El tratamiento antibiótico es un pilar en el tratamiento de esta patología. Todos los autores de este trabajo coinciden en que debe iniciarse de forma empírica siempre después de la toma de muestra para cultivo, con antibióticos de amplio espectro guiados por la epidemiología local y luego guiado según el antibiograma. Esto coincide con la bibliografía (1,3,8).
Las decisiones respecto a la selección del antibiótico, vía de administración y duración de tratamiento generalmente escapan al ortopedista y requiere la consulta con un especialista en infecciones.
En nuestra revisión analizamos la duración del tratamiento antibiótico. Todos los autores coinciden en realizar 2 etapas, primero intravenosa y luego vía oral. El paso de una a otra se valora según la respuesta clínica y paraclínica al tratamiento. La mayoría realiza este cambio según el descenso de los parámetros infecciosos y la mejoría clínica.
En nuestro medio está estipulado el uso de terapia IV por 3 semanas y luego 3 semanas VO, sabiendo que se ajusta según cada paciente pudiendo llegar en casos muy complejos a realizar terapias supresoras con tiempo indefinido(8,20). No existe un consenso internacional respecto a la duración del mismo, pero se supone que 6 semanas de tratamiento en total serian suficientes, aunque faltan estudios prospectivos (8).
TECNICA QUIRÚRGICA
La mayoría de los niños que padecen OMC han tenido múltiples intervenciones quirúrgicas (10,12,21,22). Esta situación juega un rol muy importante en el compromiso de partes blandas y la estructura esquelética, durante el proceso de tratamiento (1).
Todos los casos de OMC deben ser tratados de forma quirúrgica en asociación con antibióticos (7). Los antibióticos por si solos no son suficientes debido a la pobre cinética vascular del hueso con secuestros y fístulas. Hay descritas variadas técnicas quirúrgicas, desde simples lavajes, debridamientos locales hasta escisiones radicales, sistemas de lavado continuo, con o sin antibióticos, y procedimientos de reconstrucción usando fijadores monoplanares o dispositivos de Ilizarov (13).
Respecto al procedimiento quirúrgico utilizado se analizaron en 3 grupos:
- Limpiezas quirúrgicas y debridamiento, (LQ-D): 3 autores
- Técnica de inducción de membrana (Masquelet) asociado a LQ-D: 3 autores
- Técnicas de reconstrucción ósea asociado a LQ-D: 6 autores
La limpieza quirúrgica inicial debe ser amplia y suficiente, debe realizarse una necrectomía amplia hasta hueso sano utilizando el signo de la Paprika (6) que implica la visualización de sangrado óseo durante la cirugía.
Se utilizan distintos métodos de LQ-D: retiro de implantes, corticotomía, fresado del canal e irrigación. Se describe el método de lavado In-out (13,23) que implica el lavado del canal con suero de forma continua durante varios días. Esto implica una hospitalización prolongada y el uso de yeso lo que no permitiría valorar clínicamente al paciente.
Realizar únicamente LQ-D implica que en la misma no se generó un defecto óseo, lo que no requeriría un procedimiento de reconstrucción. Esto sólo podría lograrse si la infección no involucra toda la cortical ósea, ya que si es una infección Cierny-Mader tipo IV debería realizarse una resección amplia hasta hueso sano(7), guiándonos por el método de la paprika como dijimos previamente.
Debemos resaltar que todos los autores de este trabajo insisten en que el paso inicial en el manejo de esta patología es realizar LQ-D. Luego de esto es que pueden asociar: osteosíntesis, uso de espaciadores de cemento y procedimientos de reconstrucción. Pero siempre el paso inicial implica una conducta quirúrgica de limpieza y debridamiento radical hasta hueso sano.
3 autores analizan por separado la técnica de inducción de membrana de Masquelet. Tradicionalmente esta cirugía se realiza en 2 etapas, en la primera se utiliza un espaciador de cemento con antibióticos para rellenar el defecto óseo y en la segunda se procede a rellenar el defecto con injerto óseo (24). Realizan la segunda etapa quirúrgica cuando se normalizan los parámetros infecciosos, a las 4 semanas (16,18) u 8 semanas (17) variando según el autor. 6 semanas se supone que sería el tiempo suficiente para formar la membrana (24).
El uso de yeso de protección u osteosíntesis (clavos de kirschner o steinmann) varía entre los autores, la indicación de osteosíntesis es “si es necesario” (16–18). Creemos que es debido al defecto óseo y su estabilidad intrínseca, pero no está especificado en los artículos. No asocian fijación externa en ningún caso.
En general en los pacientes en que se realiza la técnica de Masquelet tuvieron buena evolución, sin reintervenciones. Se logró la consolidación ósea y se destaca que los niños generan una membrana perióstica más rápido que los adultos (16,18).
Al valorar los resultados según procedimiento de reconstrucción, fue imposible de analizarlos en conjunto dada la diversidad y tipos de trabajos.
No pudimos sacar conclusiones de los mismos como técnica individual. Lo que si podemos decir es que hay distintas técnicas quirúrgicas y la indicación de las mismas varía de autor y de cirujano.
El uso de injerto con sustituto óseo en una etapa(15) tuvo 100% de efectividad pero es un trabajo patrocinado por una marca comercial y tiene muy poco seguimiento de sus pacientes. Debería hacerse un grupo de control para valorar realmente la utilidad y ventajas de este sustituto óseo, con el que actualmente no contamos en nuestro medio.
La técnica más original de esta revisión implica el uso de músculo (25) para rellenar el defecto óseo con el que se logra una mejor llegada del antibiótico al sector. Esta técnica tuvo una muy buena evolución con seguimiento a 3 años. Aunque es una cirugía técnicamente compleja, se recomienda en OMC de tibia distal en el que haya poca cobertura de partes blandas.
Por último se analizan pacientes en los que se utilizo la técnica de osteogénesis por distracción siguiendo el método Ilizarov con fijadores circulares. Los autores utilizan esta técnica cuando la resección ósea es amplia y se pierde la estabilidad mecánica, aunque no especifican el tamaño del defecto. Es una técnica versátil que implica una alta curva de aprendizaje y que permite tratar la infección y a su vez las complicaciones de la misma. Ellos concluyen que es el método de preferencia cuando el resto de las técnicas fallan (10,21,22). Es útil para manejar dismetrías y angulaciones (26).
CONCLUSIONES
El manejo de las osteomielitis crónicas debe estar dado por un equipo multidisciplinario y debe estar basado en el tratamiento antibiótico dirigido al germen y el tratamiento quirúrgico planificado.
Deberían evitarse los manuales y protocolos en el tratamiento quirúrgico de estos pacientes. No encontramos superioridad en el uso de una técnica u otra pero podemos afirmar que la primera etapa quirúrgica siempre debe incluir debridamiento radical hasta hueso sano, seguido por una etapa de reconstrucción. En esta revisión los autores utilizan diversas técnicas quirúrgicas de las que se destacan la Técnica de Masquelet de inducción de membrana y el uso de fijadores externos para reconstruir defectos óseos.
BIBLIOGRAFÍA
- Herring JA. Tachdjian´s Pediatric Orthopaedics. 5a ed. ElSevier; 1976; P 1024-1052.
- Violas P, Rabier V, Marleix S, Chapuis M, Fraisse B. Infecciones osteoarticulares del niño. In: Enciclopedia Medico Quirurgica [Internet]. Elsevier; 2009. p. 1–14. Available from: http://dx.doi.org/10.1016/S1286-935X(09)70901-3
- S K. Osteomyelitis. In: RM K, RE B, HB J, BF S, editors. Nelson Tratado de Pediatria. 19th ed. Barcelona: Elsiever; 2013. p. 2471–5.
- Zunino C, Vomero A, Pandolfo S, Gutiérrez C, Algorta G, Pírez C. Etiología y evolución de las infecciones osteo-articulares 2009-2015. Hospital Pediátrico del Centro Hospitalario Pereira Rossell, Uruguay. 2015;235–42.
- Staheli L. Ortopedia pediátrica. 2a ed. Lippincott Williams & Wilkins; 2003. 287–304 p.
- Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in Long Bones. J Bone Jt Surg. 2004;86-A(10):2305–18.
- Vaeza E. Ortopedia y Traumatología. Montevideo: Oficina del Libro, FEFMUR; 2010. 355–368 p.
- Cierny G, Mader JT, Penninck JJ. CLASSIC A Clinical Staging System for Adult Osteomyelitis. 2002;7–24.
- Howard-Jones AR, Isaacs D. Systematic review of systemic antibiotic treatment for children with chronic and sub-acute pyogenic osteomyelitis. J Pediatr Child Heal. 2010;46:736–41.
- Bauer R, Kerschbaumer F, Poisel S. Vias de Abordaje e Infecciones. In: Cirugía Ortopédica. 1998. p. 330–41.
- Andreacchio A, Alberghina F, Paonessa M, Cravino M, Rosa V De, Canavese F. Tobramycin-impregnated calcium sulfate pellets for the treatment of chronic osteomyelitis in children and adolescents. J Pediatr Orthop. 2018;00(00):1–7.
- Bar-On E, Weigl D, Bor N. Chronic Osteomyelitis in Children?: Treatment by Cement Rods. J Pediatr Orthop. 2010;30(5):508–13.
- Canavese F, Corradin M, Khan A, Mansour M. Successful treatment of chronic osteomyelitis in children with debridement , antibiotic-laden cement spacer and bone graft substitute. Eur J Orthop Surg Traumatol. 2017;27:221–8.
- Felden A, Badina A, Glorion C. The Induced Membrane Technique for Bone Defects of Critical Size After Infection in Children. J Bone Jt Surg. 2016;6(3):1–5.
- Hoang NT, Staudenmaier R, Feucht A. Effectiveness of Free Gracilis Muscle Flaps in the Treatment of Chronic Osteomyelitis With Purulent Fistulas at the Distal Third of the Tibia in Children. J Pediatr Orthop. 2009;29(3):305–11.
- Mantero, E; Carbone, M; Calevo, M G; Boero S. Diagnosis and treatment of pediatric chronic osteomyelitis in developing countries?: prospective study of 96 patients treated in Kenya. Musculoskelet Surg. 2011;13–8.
- Matzkin EG, Dabbs DN, Fillman RR, Kyono WT, Yandow SM. Chronic osteomyelitis in children?: Shriners Hospital Honolulu experience. J Pediatr Orthop B. 2005;14(5):362–6.
- Rousset M, Walle M, Cambou L, Mansour M, Samba A, Pereira B, et al. Chronic infection and infected non-union of the long bones in paediatric patients?: preliminary results of bone versus beta-tricalcium phosphate grafting after induced membrane formation. Int Orthop. 2017;42(2):385–93.
- BK S, T R, B B, AK B. Surgical interventions in chronic osteomyelitis. Kathmandu Univ Med J. 2005;3(9):50–4.
- Unal V, Dayican A, Demirel M. Selection of treatment modalities in children with chronic osteomyelitis. Acta Orthop Traumatolgica Turc. 2006;40(1):56–61.
- Wirbel R, Hermans K. Surgical treatment of chronic osteomyelitis in children admitted from developing countries. African J Paediatr Surg. 2014;11(4):297–304.
- Yeargan III, Austin; Nakasone, Cass; Shaieb M. Treatment of Chronic Osteomyelitis in Children Resistant to Previous Therapy. J Pediatr Orthop. 2004;24(1):109–22.
- Krogstad P. Osteomyelitis. In: Feigin RD Cherry JD, Demmler-Harrison GL, Kaplan SL Feigin and Cherry?s TextBook of Pediatric Infectious Diseases. 6a ed. Elsevier; 2009. p. 725–42.
- Cuneo A, Pírez C, Giachetto G, Galiana A. Protocolo de Estudio y Tratamiento de Infecciones Osteo-articulares en Pacientes Pediátricos. Uruguay: www.ortoped.fmed.edu.uy; 2009.
- Masquelet AC, Begue T. The Concept of Induced Membrane for Reconstruction of Long Bone Defects. Orthop Clin North Am [Internet]. 2010;41(1):27–37.
