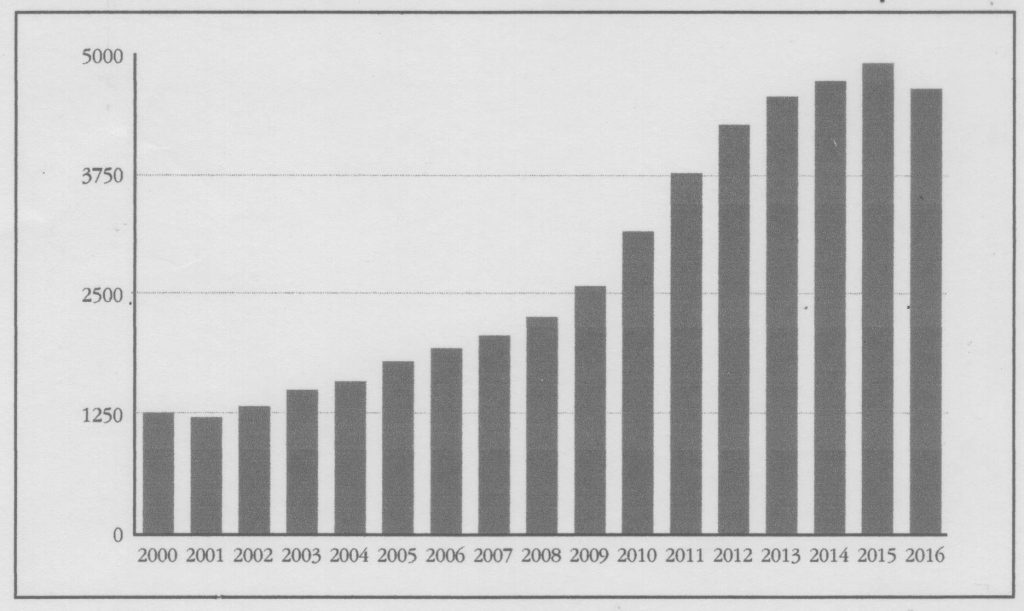
El interés por la vitamina D ha ido en aumento en los últimos años, lo que se ve expresado en el número de artículos publicados en revistas recogidas por la base de datos “PubMed”. Se han multiplicado casi por 4 desde el año 2000 al 2016 como lo ilustra la Fig. 1, trabajo realizado por el Prof. Manuel Díaz Curiel del Hospital Jiménez Díaz de Madrid.
La vitamina D mantiene su nombre desde su descubrimiento por Mc Collum en 1922, designándola “D” por ser la cuarta en descubrirse (1). Es en realidad un complejo sistema hormonal (2), siendo su estructura muy parecida a la de las hormonas esteroideas y el propio Mc Collum afirmó que esta vitamina antirraquítica tenía propiedades específicas en la regulación del metabolismo óseo.
La hormona D, como la deberíamos denominar (3), comenzó a estudiarse y a relacionarse con el metabolismo mineral óseo, siendo conocido que su déficit produce una enfermedad esquelética que es denominada raquitismo en los niños y osteomalacia en los adultos (4). Fue Trousseau en 1861, el primero en vincular al raquitismo con una carencia a la exposición al sol asociada a una dieta defectuosa y que el aceite de hígado de bacalao podía curarlo (5).
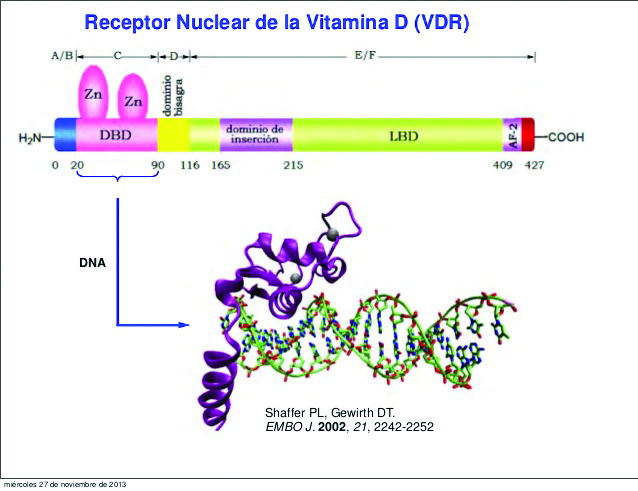
En el siglo XX, se comprobó que prácticamente todas las células del organismo tienen receptores para esta hormona (VDR) Fig. 2, ampliándose su conocimiento en otros aspectos fisiopatológicos y clínicos, tanto en la osteoporosis (6), (7), como en otras enfermedades distintas a las óseas. A la relación de la vitamina D con estos procesos se ha denominado “efectos extraóseos de la vitamina D o pleiotrópicos”.
Actualmente conocemos mejor la relación de la vitamina D con los músculos y las caídas, con la diabetes mellitus, tanto tipo 1 como 2 (8), con la hipertensión arterial y la cardiopatía isquémica (9), el sistema inmunitario y las enfermedades autoinmunes (10), las infecciones respiratorias (11), el asma bronquial (12) o el cáncer (13), sobre los que se han publicado un mayor número de artículos.
El viejo concepto que solo el riñón activa la vitamina D ha cambiado no solo por encontrar receptores de D3 (VDR) sino, además, por haberse identificado la enzima 1 alfa hodroxilasa en múltiples tejidos y a nivel celular como macrófagos y linfocitos, consiguiéndose un elevado nivel intracelular y tisular que muchas veces no es el reflejo del nivel plasmático. Recordemos que lo que medimos en sangre es la 25 (OH) D3 (Calcidiol) y no la 1-25 (OH) D3 (Calcitriol) la que tiene una vida media muy corta entre 4 a 6 horas.
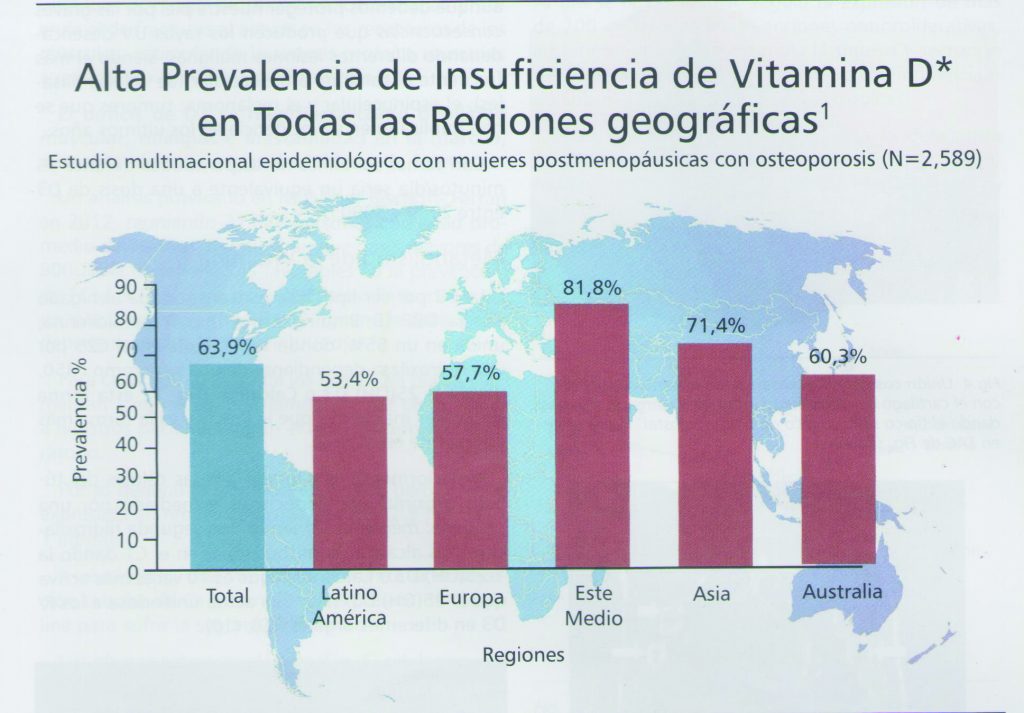
A nivel mundial hay una alta prevalencia de insuficiencia de D3 que oscila entre el 60% a 80%, Fig. 3. Se ha determinado que los niveles normales deberían estar entre 30 y 100 ngrs/ml, entre 20 y 29 ngrs correspondería a una insuficiencia y por debajo de 19 ngrs una deficiencia.
Al ser activada tiene efectos calciotrópicos y no calciotrópicos. Entre los primeros aumenta el transporte transepitelial de Calcio (Ca) a nivel intestinal con efectos directos a nivel óseo aumentando la mineralización, el remodelado óseo a través del RANKL/Osteoprotegerina y aumenta la síntesis del factor FGF23 (Factor de crecimiento fibroblástico) que regula los niveles del fosforo plasmático. Disminuye la reabsorción ósea inducida por la PTH, aumenta la formación ósea cortical y trabecular por estimular la actividad de los osteoblastos (OB) y expresar la 1 alfa hidroxilasa promoviendo la reparación de las microfracturas. El déficit de D3 estimula la osteoclastogénesis con un balance negativo por aumentar la actividad de los osteoclastos.
Estos efectos se traducen en un aumento en la densidad mineral ósea (DMO), la cual podemos evaluar a través de la Densitometría (DXA) por centímetro cuadrado o cúbico del hueso.
A nivel renal aumenta la reabsorción tubular de Ca y de megalina para sufrir la segunda hidroxilación por la hidroxilasa (CYP24A1). Actuando a nivel de las paratiroides disminuye en tenor de PTH.
Como efectos no calciotrópicos de la D3, es una reguladora de la secreción hormonal aumentando la síntesis de insulina y disminuyendo el nivel de renina, por lo que tiene incidencia directa en patologías como la diabetes y la hipertensión (8), (9). A nivel inmunológico es un verdadero inmunomodulador actuando tanto en la inmunidad innata y en la adquirida, como lo veremos más adelante. En el ámbito celular actúa en el remodelado celular, con efectos antiproliferativos por actuar regulando la expresión de más de 200 genes y prodiferenciador. Estos mecanismos explicarían que su deficiencia o insuficiencia aumentan los riesgos de enfermedades autoinmunes, infecciosas, diabetes, hipertensión y cáncer.
Efectos inmunomoduladores
La D3 actúa directamente a nivel de las uniones celulares a través de la E cadherina en las uniones adherensjunctions y por medio de la conexina 43 en el gapjunctions ejerciendo un verdadero efecto de barrera para bacterias y virus los que alteran la misma (14), (15).
Ya hemos mencionado que las células inmunes expresan VRD y tienen enzimas para sintetizar la 1-25 (OH) D3, la cual induce la formación de proteínas antimicrobianas como la defensina y cathelicidina. Camargo en 2011 (16) realizó los primeros reportes vinculando la asociación inversa entre los niveles deficitarios de D3 y el riesgo de infecciones respiratorias de origen viral. Estas observaciones han sido corroboradas por otros autores como Belderbos, M.E. (2011) en Holanda, Morales, E. (2012) en 1693 niños, Chawes, B.L. (2016) en Dinamarca en 581, aumento de cuadros respiratorios virales en los insuficientes de D3.
Tiene además efectos directos sobre los linfocitos T helpers inhibiendo la síntesis de citoquinas proinflamatorias, TNF e interferón gama, por lo que hay una relación inversa entre los déficits de D3 y las enfermedades virales, incluso hasta del virus de la pandemia actual que produce el COVID-19, donde el pronóstico de la neumonía es más desfavorable si los pacientes tienen una D3 por debajo de 30 ngrs/ml (17), (18).
D3, diabetes y síndrome metabólico (SM)
Los niveles de D3 están inversamente asociados con la presencia de SM, confirmado en varios estudios epidemiológicos; se postula un secuestro de la vitamina en el exceso de tejido adiposo reduciendo su biodisponibilidad (19) y desempeñando un papel en la resistencia a la insulina (IN) característica en este síndrome, Fig. 4.
Corrigiendo la deficiencia podría mejorar la sensibilidad a la IN aumentando la expresión de sus receptores (20). Varios estudios y un metaanálisis de 21 trials prospectivos demostraron una asociación inversa entre DM2 y los niveles bajos de D3 (21) que se asociaría a un deterioro de la función de las células betas. El aumento de la PTH en estos casos deficitarios de D3 estimula la adipogénesis y a la diferenciación de preadipocitos.
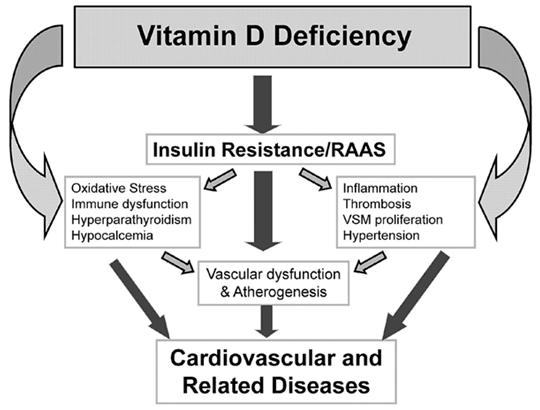
En la Fig. 4 se ilustran los mecanismos de la deficiencia de D3 con la patología cardio vascular donde los niveles elevados de PTH se correlacionan con un aumento del riesgo CV, hipertensión arterial confirmada desde los trabajos de Resnick, L.M. (22), describiéndose VDR en las células musculares lisas (CML) vascular y en los cardiomiocitos. La deficiencia se ha correlacionado a un aumento de la mortalidad CV.
Vitamina D3 a nivel del SNC
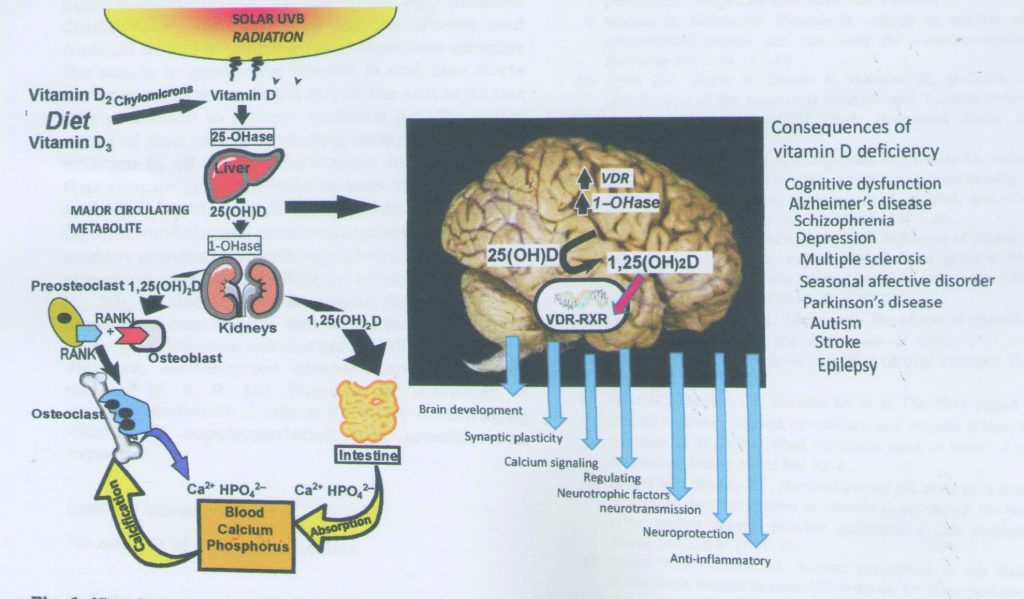
Se han determinado también VDR en el SNC, Fig. 5, donde su deficiencia lleva a una disminución de la neuroplasticidad (dendrogénesis y sinaptogénesis) por disminuir la regulación del factor neurotrófico cerebral (BDNF) que se ve estimulada por la D3 y se vincula además con patologías como Alzheimer, Depresión, Parkinson, disminución del nivel cognitivo, entre otras, donde la regulación del Ca tiene su directa incidencia (23).
Causas de deficiencia e insuficiencia de D3
La falta de exposición a la luz solar, el envejecimiento de la piel brindando menos precursores (7-dihidrocolesterol) a tenerlo muy en cuenta en pacientes gerontes. La latitud geográfica del Uruguay a 33 grados. Por déficit enzimático en hepatopatías donde disminuya la actividad del 1 alfa hodroxilación. En síndromes mal absortivos también llevan a un déficit de D3. La obesidad de los pacientes diabéticos y con SM secuestrando la D3. En pacientes que cursan nefropatías crónicas donde hay una deficiencia de la segunda hidroxilación. En mutaciones del gen VDR en cuyos niveles de D3 llegan a ser indetectables, como la paciente de la Fig.6. Los pacientes afrodescendientes presentan con frecuencia déficit de D3 porque la melanina es una pantalla natural para los rayos UV. El uso indiscriminado de protectores solares, un protector factor 30 disminuye más del 80% la activación de D3. Una causa frecuente también de D3 deficitaria es en los pacientes que cursan hipomagnesemia por causas gastrointestinales, renales, en la glucosuria en los diabéticos y usos abusivos de diuréticos.

Reposición y suplementación de D3
Podríamos manejar una matemática de D3; puede venir expresada en ngrs/ml que sería lo más frecuente, aunque a veces la expresan en nmol/L.
2.5 nmol/L equivale a 1 ngr/ml.
Por lo tanto, si la informan en nmol debemos dividir en 2.5 para expresarla a ngrs/ml.
Debemos tener presente que por cada 100 UI ingerida los niveles sanguíneos aumentarán en 1 ngr, dependiendo de la edad del paciente, ya que en aquellos de edad más avanzada la absorción intestinal está disminuida.
Una fórmula muy práctica para aplicar en la rutina diaria de nuestras consultas es que por cada ngr a reponer se multiplica x 140 si es D3 o x 280 si se maneja D2 dando la dosis diaria a prescribir y si al resultado lo multiplicamos por 7 nos da la dosis semanal.
Ejemplo: en un paciente nos informan que tiene 14 ngrs/ml y deberíamos llegar al nivel mínimo considerado normal 30 ngrs, restamos 30-14= 16.
16 x 140= 2240 UI/día.
2240 x 7= 15.860UI/ semana, parecieran dosis altas, pero no hay riesgos de efectos colaterales como lo han demostrado varios autores como Amir (24), (25), Shirvani (26).
Aplicado esta fórmula no corremos riesgos de manejar dosis que puedan superar los 100 ngrs/ml, evitando la toxicidad y corroborando, titulando con controles cada 6 meses en laboratorios confiables y con experiencia en determinar 25(OH)D3.
En algunos casos con niveles muy bajos, déficit severo, se podría suplementar con una “dosis carga” y posterior dosis de mantenimiento (27), pero se han reportado que se puede llegar a 30 ngrs/ml con posología diaria, semanal o incluso mensual y dependiendo de la patología a tratar. Es diferente suplementar D3 para una paciente con osteoporosis que suplementar a una que cursa COVID-19, tal como lo menciona Mansur, J.L de La Plata (Argentina). Por lo general en los diferentes consensos no se han recomendado las megadosis (Consensos de Panamá, de Colombia, 2019), salvo casos puntuales con déficit severos y con los cuidados pertinentes en hipercalcemias y se han reportado riesgos aumentados de caídas. Para los pacientes obesos en DM2 y SM el aporte debe ser 2 a 3 veces mayor a la dosis calculada (28), por el fenómeno de secuestro en tejido adiposo, antes mencionado.
Bibliografía
(1) Mc Collum et all. Studies on experimental rickets. The production of rachitis and similar diseases in the rat by deficient diets. J. Biol. Chem. 1921; 45:333-342.
(2) Bischoff-Ferrari H. Vitamin D – from essentiality to functionality. Int J VitamNutr Res. 2012;82(5):321-326,
(3) Norman AW. From vitamin D to hormone D – fundamentals of the vitamin D system. Am J ClinNutr. 2008;88(suppl):491s-9s.
(4) Holick M. Vitamin D deficiency. N Engl J Med. 2007; 357(3):266-81.
(5) Trousseau, A.Cliniquemédicalede l’ Hotel Dieu de Paris. Balliere et fils. 1973,3:490-532.
(6) Holick MF. High prevalence of vitamin D inadequacy and implications for health. Mayo Clin Proc. 2006;81(3):353-73.
(7) Holick MF. Resurrection of vitamin D and rickets. J Clin Invest. 2006;116(8):2062-72.
(8) Al-Timimi DJ, Ali AF. Serum 25(OH) D in diabetes mellitus type 2: relation to glycaemic control. J Clin Diagnostic Res. 2013;7(12):2686-8.
(9) Alkhatatbeh MJ, Abdul-Razzak KK, Khasawneh LQ, Saadeh NA. High prevalence of vitamin D deficiency and correlation of serum vitamin d with cardiovascular risk in patients with metabolic syndrome. MetabSyndrRelatDisord. 2017 Mar 27. Epub ahead of print.
(10) Broder AR, Tobin JN, Putterman C. Disease-specific definitions of vitamin D deficiency need to be established in autoimmune and non-autoimmune chronic diseases: a retrospective comparison of three chronic diseases. Arthritis Res Ther. 2010;12(5):1-8.
(11) Martineau A, Jolliffe D, Hooper R, Greenberg L, Aloia J, Bergman P, et al. S102 Vitamin D supplementation to prevent acute respiratory infections: systematic review and meta-analysis of individual participant data. Thorax. 2016;71(Suppl 3): A60-1.
(12) Kim Y-R, Seo S-C, Yoo Y, Choung JT. Are children with asthma in south korea also associated with vitamin D deficiency? Environ Health Toxicol. 2017;1-7.
(13) Acevedo F, Pérez V, Pérez-Sepúlveda A, Florenzano P, Artigas R, Medina L, et al. High prevalence of vitamin D deficiency in women with breast cancer: the first Chilean study. The Breast. 2016; 29:39-43.
(14) Schwalfenberg, G.K. A review of the criticalrole of vitamin D in the functioning of the immune system and the clinical implications of vitamin D deficiency. Mol. Nutr. Food Res. 2011,55,96-108. DOI: 10.1155/2018/5813095.
(15) Kast; J.I. et all. Respiratory syncytial virus infection influences tight junction integrity. Clin. Exp. Inmunol. 2017; 190:351-359. DOI: 10.1111/cei. 13042.
(16) Camargo, C. A. et all. Cord blood 25(OH)D3 levels and risk of repiratory infection, wheezing and asthma. Pediatrics 2011; 127 (1): e180-e187.
(17) Theron, M. et all.A probable role for IFN gama in the development of a lung immunopathology in SARS. Cytokine 2005, 32,30-38. DOI: 10.1016/j.cyto.2005.07.007.
(18) Huang, C. et all. Clinical features of patients infected with 2019 novel coronavirus in Wuhan. Lancet 2020, 10.1016/S0140-6736 (20) 30183-5.
(19) Wortsman J, Matsuoka LY, Chen TC, Lu Z, Holick MF. Decreased bioavailability of vitamin D in obesity. Am J ClinNutr 2000; 72:690-3.
(20) Talaei A, Mohamadi M, Adgi Z. The effect of vitamin D on insulin resistance in patients with type 2 diabetes. DiabetolMetabSyndr 2013; 5:8.
(21) Song Y, Wang L, Pittas AG, et al. Blood 25-hydroxy vitamin D levels and incident type 2 diabetes: a meta-analysis of prospective studies. Diabetes Care 2013; 36:1422-8.
(22) Resnick, L.M. Ann. Intern. Med. 1986, 105: 649-654.
(23) Holick, M.F. Journal of Internal Medicina 2014, 90-92. DOI:10.1111/joim.12308.
(24) Amir, E. et all. A phase 2 trial exploring the effects of high dose (10.00 IU/day) vitamin D3 in breast cancer patients with bone metastasis. Cancer 2010, 116: 284-291.
(25) Charoenngam, N et all. The effect of various doses of oral D3 supplementation on gut microbiota in healthy adults. Anticancer Res. 2020, 40: 551-556. DOI: 10.21873/anticanres.13984.
(26) Shirvani,A.; Kalajian, T.A.; Song, A.; Holock, M.F. Disassociation of vitamin D calcemic activity and non-calcemic genomic activity and individual responsiveness. Sci. Rep. 2019,9: 17685. DOI: 10.1038/s41598-019-53864-1.
(27) Mansur J.L. Suplementar con vitaminaD3 para prevenir o tratar la infección por coronavirus (COVID-19) puede ser de utilidad?Webinar, 2020.
(28) Ekwaru, J.P. et all. The supplementation and serum 25(OH) D in healthy volunteers. PloS One 2014, 9: e11625. DOI: 10.1371/journal.pone.0111265.

Dr. Edgardo Romero Galván
Doctor en Medicina, Universidad de la República 1984.
Especialista en Oncología Médica. Universidad de la República, 1998.
Postgrado en Diagnóstico y Tratamiento del Dolor Universidad de Buenos Aires (1999) y Barceló (2009) Buenos Aires.
Diplomado en Lipidología. UBA/FEPREVA, Buenos Aires, 2011.
Diplomado en Metabolismo Mineral Óseo, Universidad Autónoma de Baja California.


